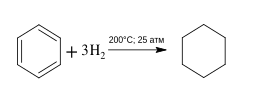Циклоалканы
Циклоалка́ны (также полиметиленовые углеводороды[1], нафтены, цикланы, или циклопарафины) — циклические насыщенные углеводороды, образующие гомологический ряд с общей формулой CnH2n. Все атомы углерода в циклоалканах находятся в sp3-гибридизированном состоянии.[2] Простейшим циклоалканом является циклопропан(С3H6).
Входят в состав нефти. Открыты В. В. Марковниковым в 1883 году из бакинской нефти[3]
Номенклатура и изомерия
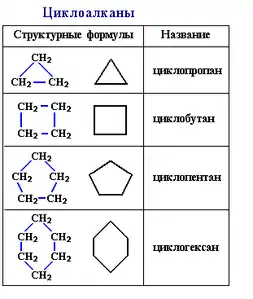
Названия циклоалканов строятся из названий соответствующих алканов с добавлением приставки цикло- (циклопропан, 1,3-диметилциклогексан, циклобутан, циклопентан).
Для циклоалканов характерны следующие виды изомерии:
- Изомерия углеродного скелета: циклобутан, 1-метилциклопропан и т.д.
- Пространственная. Для циклоалканов характерна цис-транс-изомерия: если два заместителя находятся по одну сторону цикла, то этот изомер называется цис-изомером, если же два заместителя находятся по разные стороны от цикла, то изомер называется транс-изомером.[2]
- Межклассовая изомерия с алкенами.
Классификация
Циклоалканы делятся на моноциклические и бициклические циклоалканы.
В свою очередь, бициклические циклоалканы делятся на спироалканы и бициклоалканы:
- Спироалканы - углеводороды, состоящие из двух циклов, в которых один углеродный атом является общим(узловым). Представителем спироалканов является спиропентан. Название образуется путем добавления приставки спиро-, указанием количества нецентральных атомов в циклах в квадратных скобках и путем добавления окончания соответствующего алкана. Например, для спиропентана это название будет спиро[2.2]пентан.
- Бициклоалканы - углеводороды, состоящие из двух циклов, в которых два углеродных атома являются общими. Название получается путем добавления приставки бицикло-, указанием количества нецентральных атомов в циклах в квадратных скобках и путем добавления окончания соответствующего алкана. Например, для бициклобутана это название будет бицикло[1.1.0]бутан.[2]
Физические свойства
Все атомы углерода в молекулах циклоалканов имеют sp³-гибридизацию. Однако величины углов между гибридными орбиталями в циклобутане и особенно в циклопропане не 109°28', а меньше из-за геометрии, что создаёт в молекулах напряжение, поэтому малые циклы очень реакционноспособны.
При обычных условиях первые два члена ряда (C3 — C4) — газы, (C5 — C11) — жидкости, начиная с C12 — твёрдые вещества. Температуры кипения и плавления циклоалканов выше, чем у соответствующих алканов. Циклоалканы в воде практически не растворяются. При увеличении числа атомов углерода возрастает молярная масса, следовательно, увеличивается температура плавления.
Температуры плавления и кипения некоторых циклоалканов: [4]
| Циклоалкан | Т. пл., °C | Т. кип., °C |
|---|---|---|
| циклопропан C3H6 | −127 | −33 |
| циклобутан C4H8 | −90 | 13 |
| циклопентан C5H10 | −94 | 49 |
| циклогексан C6H12 | 7 | 81 |
| циклогептан C7H14 | −8 | 119 |
| циклооктан C8H16 | 15 | 151 |
| циклононан C9H18 | 11 | 178 |
Получение
Циклоалканы в значительном количестве находятся в нефти, а также содержатся в природных соединениях.[2]
Металлорганический синтез
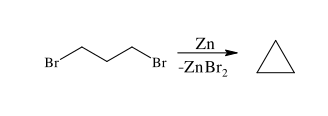
Циклоалканы можно получить дегалогенированием дигалогенпроизводных (металлорганический синтез) при помощи магния, натрия или цинка:
Каталитическое гидрирование бензола и его гомологов приводит к образованию циклогексана или его производных):
В данной реакции катализатором может служить никель Ренея, никель, платина, палладий.[5]
Химические свойства
По химическим свойствам малые и обычные циклы существенно различаются между собой. Циклопропан и циклобутан склонны к реакциям присоединения, то есть сходны в этом отношении с алкенами. Циклопентан и циклогексан по своему химическому поведению близки к алканам, так как вступают в реакции замещения.
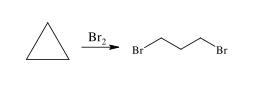
- Циклопропан и циклобутан способны присоединять бром:
- Также циклопропан и циклобутан могут присоединять галогеноводороды, присоединение происходит с раскрытием цикла, по правилу Марковникова.[6]
- Циклопропан, циклобутан и циклопентан могут присоединять водород, давая соответствующие нормальные алканы. Присоединение происходит при нагревании в присутствии никелевого катализатора:
Применение
В нефтехимической промышленности нафтены являются источником получения ароматических углеводородов путём каталитического риформинга. Наибольшее практическое значение приобрёл циклогексан, применяемый для синтеза капролактама, адипиновой кислоты и других соединений, используемых в производстве синтетического волокна.
Циклопропан применяют для наркоза, но его применение ограничено из-за взрывоопасности.
Примечания
- Полиметиленовые углеводороды // Большая советская энциклопедия : [в 30 т.] / гл. ред. А. М. Прохоров. — 3-е изд. — М. : Советская энциклопедия, 1969—1978.
- Valerij Fedorovič. Traven'. Organičeskaâ himiâ : v treh tomah. 1. — 2-e izd., pererab. i dop. — Moskva: BINOM. Laboratoriâ znanij, cop. 2013. — С. 196. — 368 s. с. — ISBN 978-5-9963-0406-6, 5-9963-0406-6, 978-5-9963-0357-1, 5-9963-0357-4.
- Владимир Васильевич Марковников (1838-1904) [1948 - - Люди русской науки. Том 1]. nplit.ru. Дата обращения: 21 ноября 2015.
- Робертс Дж., Касерио М. Основы органической химии. В 2 томах = Basic Principles of Organic Chemistry / Пер. с англ. Ю. Г. Бунделя, под ред. А. Н. Несмеянова. — 2-е изд., дополненное. — М.: Мир, 1978. — Т. 1. — 121 с.
- Valerij Fedorovič. Traven'. Organičeskaâ himiâ : v treh tomah. 1. — 2-e izd., pererab. i dop. — Moskva: BINOM. Laboratoriâ znanij, cop. 2013. — С. 198. — 368 s. с. — ISBN 978-5-9963-0406-6, 5-9963-0406-6, 978-5-9963-0357-1, 5-9963-0357-4.
- Г.И. Дерябина, Г.В. Кантария, Д.И. Грошев. Свойства циклоалканов. Интерактивный мультимедиа учебник "Органическая химия".
Литература
- Кузьменко Н. Е., Еремин В. В., Попков В. А. Начала химии. Современный курс для поступающих в вузы.. — М.: Экзамен, 2002.