Фавипиравир
Фавипирави́р — нуклеозидный аналог, разработанный и лицензированный в Японии для лечения гриппа в условиях новых пандемий[1][2].
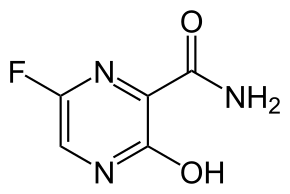
| Фавипиравир | |
|---|---|
 | |
| Химическое соединение | |
| ИЮПАК | 6-фторо-3-гидроксипиразин-2-карбоксамид |
| Брутто-формула | C5H4FN3O2 |
| Молярная масса | 157,104 г/моль |
| CAS | 259793-96-9 |
| PubChem | 492405 |
| DrugBank | 12466 |
| Состав | |
| Классификация | |
| АТХ | J05AX27 |
| Способы введения | |
| перорально | |
| Другие названия | |
| Фавилавир, Авифавир, Авиган, Арепливир, Коронавир, T-705 | |
До получения международного непатентованного названия фавипиравир обозначался индексом разработчика T-705[2]. Первые публикации о препарате появились в 2002 году[3].
Фавипиравир для лечения гриппа зарегистрирован только в Японии, в других странах его применимость против гриппа и других заболеваний исследуется[4][5].
Фавипиравир исследовался как возможное средство против SARS-CoV-2, попал в руководства по лечению некоторых стран[6][7]. В 2020 году он зарегистрирован в России и включен в список жизненно необходимых и важнейших лекарственных препаратов Минздрава России[8]. На конец 2021 года имеются доказательства его неэффективности при COVID-19[9].
Фармакологические свойства
Фармакодинамика
In vitro фавипиравир обладает широким спектром активности против РНК-содержащих вирусов, включая вирусы гриппа, риновирус, респираторно-синцитиальный вирус, а также опасных для жизни вирусы. Не работает против ДНК-содержащих вирусов, в числе которых аденовирус, вирус простого герпеса первого типа и цитомегаловирус[2].
Механизм действия
О механизме действия фавипиравира есть разные мнения. Одни исследователи считают, что фавипиравир селективно ингибирует вирусную РНК-зависимую РНК-полимеразу[10]. Другие исследования показывают, что фавипиравир индуцирует летальные мутации РНК-трансверсии, производя нежизнеспособный вирусный фенотип[11] путём терминирования удлинения формирующейся цепи РНК[2].
Также есть мнение, что фавипиравир как в пероральной, так и внутривенной формах является пролекарством, которое метаболизируется до его активной формы, фавипиравир-рибофуранозил-5'-трифосфат (фавипиравир-RTP)[12][13]. Считается, что человеческая гипоксантин-гуанин-фосфорибозилтрансфераза (HGPRT) играет ключевую роль в процессе его активации[14].
Применение в медицине
Фавипиравир был одобрен для лечения гриппа в Японии[15]. Однако он показан только для нового гриппа (штаммы, вызывающие более тяжёлые заболевания), а не для сезонного гриппа[15]. По состоянию на 2020 год вероятность развития резистентности представляется низкой[15].
В России фавипиравир включен в рекомендации по лечению COVID-19[8].
Побочные эффекты
На начало 2020 года Фавипиравир считался относительно безопасным препаратом. Однако исследования показали, что он может приводить к дозозависимому повышению уровня мочевой кислоты в крови — гиперурикемии. Пока что нет никаких доказательств возможных клинических проявлений вызванной фавипиравиром гиперурикемии, хотя при более длительном курсе лечения они не исключаются. Также есть предположения о возможном увеличении интервала QT под действием фавипиравира, однако для подтверждения или опровержения этого требуются дополнительные исследования
Имеющиеся на начало 2020 года доказательства предполагают безопасность и хорошую переносимость препарата при краткосрочных курсах лечения, однако безопасность фавипиравира при длительном использовании к 2020 году не была изучена[16].
На 2021 год известно, что фавипиравир вызывает накопление мочевой кислоты в крови[17], это было выяснено к 2020 году, но тогда не было известно, приводит ли это к негативным последствиям[16]. Фавипиравир токсичен при беременности и планировании беременности, он способен нарушить эмбриональное развитие плода[17].
Приём фавипиравира во время беременности может нанести вред будущему ребёнку[18][19]. Эксперименты на 4 видах животных показали замедленное развитие эмбриона и его смерть в первом триместре, однако исследования на людях, включающие беременных или кормящих женщин, отсутствуют. В связи с риском тератогенности Японское бюро по безопасности лекарственных средств (англ. Pharmaceuticals and Medical Devices Agency) ввело строгие ограничения для использования препарата среди женщин репродуктивного возраста и предписало производителю указывать предупреждение об этом на упаковках и в инструкциях. Фавипиравир разрешено использовать в Японии только при отсутствии альтернатив[16][20].
История
Фавипиравир разработан в 2002 году[17] японской компанией FUJIFILM Toyama Chemical Co., Ltd.[9]. В разработавшей препарат компании Toyama Chemical тогда надеялись, что фавипиравир станет новым лекарством от гриппа, которое может заменить осельтамивир, но эксперименты на животных показали, что он может негативно влиять на ДНК будущего ребёнка с риском повреждения плода, поэтому одобрение данного препарата Министерством здравоохранения, труда и социального обеспечения Японии было отложено на неопределённый срок[21].
В 2014 году фавипиравир был одобрен в Японии в качестве препарата против гриппа[22] — ограниченно разрешён для лечения гриппа A и B, вызванного резистентными к противовирусным препаратам штаммами[23], и не предназначен для лечения сезонного гриппа. По состоянию на 2020 год вероятность развития резистентности вируса гриппа к препарату остаётся низкой[18].
15 марта 2020 года препарат был разрешён к продаже в Китае для лечения гриппа[24]. 30 мая 2020 года фавипиравир, выпускаемый под торговым наименованием «Авифавир» на совместном предприятии «ХимРара» и РФПИ, зарегистрирован в России как лекарство от коронавирусной инфекции[25]. До 17 сентября 2020 года[26] фавипиравир в России не был предназначен для продажи в розницу, а разрешён к применению только в условиях стационара[27]. Немецкое правительство также закупило некоторое количество фавипиравира, чтобы поставлять его в клиники по запросам врачей, но спросом у них он не пользуется. Немецкие специалисты отмечают, что в России, относительно европейских стран, ниже требования к клиническим исследованиям, необходимым для сертификации (регистрации) лекарств, а сама процедура регистрации менее строгая, чем у них[27].
В октябре 2020 года фавипиравир включен в список «Жизненно необходимые и важнейшие лекарственные препараты» (ЖНВЛП) Минздрава РФ[8].
Фавипиравир изучался как потенциальное средство для лечения коронавирусной инфекции COVID-19[28]. Он не оправдал ожиданий: в исследовании, выполненном по стандартам доказательной медицины, завершённом в середине 2020 года, значимый терапевтический эффект у него не обнаружен[29][30]. В 2021 году завершилось другое исследование фавипиравира при лечении COVID-19, в котором клинический эффект этого препарата не был обнаружен. Проводившая исследование канадская компания Appili Therapeutics, ранее вступившая в консорциум производителей фавипиравира, опубликовала заявление, в котором признала ошибочность своих надежд на эффективность фавипиравира и пообещала сосредоточиться на разработках других лекарств против COVID-19[9].
На 2020 год Фавипиравир изучается как потенциальное средство для лечения ряда других вирусных инфекций[28].
Общество и культура
Правовой статус
Министерство обороны США разработало фавипиравир в партнёрстве с MediVector, Inc. в качестве противовирусного препарата широкого спектра действия и спонсировало его в рамках клинических испытаний фазы II и III FDA, в которых он продемонстрировал безопасность для людей и эффективность против вируса гриппа[31]. Несмотря на демонстрацию безопасности более чем у 2000 пациентов и ускорение выведения вируса гриппа на 6–14 часов в неопубликованных исследованиях фазы III, фавипиравир по-прежнему не одобрен в Великобритании и США[32]. В 2014 году Япония одобрила фавипиравир для лечения штаммов гриппа, не реагирующих на современные противовирусные препараты[33]. Первоначально компания Toyama Chemical надеялась, что фавипиравир станет новым лекарством от гриппа, которое сможет заменить осельтамивир (торговая марка Тамифлю). Однако эксперименты на животных показывают потенциал тератогенных эффектов, и одобрение производства Министерством здравоохранения, труда и социального обеспечения было сильно задержано, а условия производства ограничены только в случае чрезвычайной ситуации в Японии[34].
Из-за пандемии COVID-19 фавипиравир был быстро одобрен в Китае в феврале 2020 года для розничной продажи[35][36].
20 июня 2020 года препарат был одобрен в Индии для лечения пациентов с COVID-19 под торговой маркой Fabiflu[37].
В России
29 мая 2020 года первый препарат фавипиравира зарегистрирован Минздравом РФ[38].
30 мая 2020 года Минздрав России зарегистрировал дженерик фавипиравира под названием «Авифавир»[39][40][41].
25 июня 2020 года Минздрав России одобрил второй препарат фавипиравира — «Арепливир»[42].
С июня-июля 2020 года фавипиравир доступен в России под торговыми марками «Авифавир», «Арепливир» и «Коронавир»[38][43].
Эффективность и безопасность
В 2009 году фавипиравир считался нетоксичным для млекопитающих, поскольку он не ингибирует синтез их собственных РНК или ДНК[46]. Инструкции к российским препаратам фавипиравира приводят данные об ингибировании β- и γ- ДНК-полимераз человека, а также полимеразы II РНК человека[47]. На 2014 год некоторые стандартные[48] тесты на генотоксичность (способность вызывать мутации/повреждения ДНК) на клетках и на животных дали положительный результат, однако эти результаты были объяснены непрямыми эффектами, и риск генотоксичности фавипиравира считался низким[49].
На 2020 год утверждения об эффективности фавипиравира при лечении любых болезней людей ничем не обоснованы[50][29], на август-октябрь 2021 года для него также нет доказательств эффективности[6][5].
Из-за тератогенности и эмбриотоксичности для животных фавипиравир противопоказан беременным женщинам[2].
Исследования
Препарат показал активность против многих вирусов в лабораторных условиях in vitro и некоторую эффективность в испытаниях на животных. На людях испытывался против опасных для жизни вирусов лихорадок Эбола и Ласса, вирусов бешенства и тяжелой лихорадки с синдромом тромбоцитопении. Пока отсутствуют штаммы, выработавшие устойчивость к препарату[2].
При выдаче разрешения на ограниченное использование в Японии в 2014 году PMDA указало на отсутствие полного спектра исследований препарата и предписало производителю провести их и опубликовать результаты[51].
В 2014 году некоторые исследователи высказывали предположение о потенциале фавипиравира для лечения геморрагической лихорадки Эболы[52][53]. Но проведённое впоследствии клиническое исследование в Гвинее имеет серьёзные недостатки методики и ничего не доказывает[54].
К середине 2020 года были завершены 14 клинических испытаний фавипиравира как лекарства для лечения разных заболеваний, при этом результаты опубликованы только в одном испытании 2 фазы и одном — третьей, у 12 исследований результаты недоступны для анализа. В одном исследовании второй фазы показано, что препарат клинически эффективен против вирусов гриппа, при этом отсутствовали смертность и серьёзные побочные эффекты. В другом исследовании (третьей фазы) сделан вывод, что препарат может облегчать симптомы и снижать лихорадку[55].
COVID-19
Фавипиравир изучался в качестве потенциального средства лечения COVID-19 с февраля 2020[56][57][58][59][60]. В апреле 2020 года специалисты ВОЗ отложили обсуждение включения фавипиравира в исследование Solidarity из-за недостаточности доказательств его эффективности[61].
В июле 2020 года, после завершения клинического испытания на 89 пациентах, японские исследователи в интервью сообщили, что не смогли обнаружить у фавипиравира терапевтический эффект при лечении им COVID-19[29].
В исследовании по стандартам доказательной медицины, завершившемся в Японии в 2020 году, значимый эффект применения фавипиравира в лечении COVID-19 не обнаружен[29][30].
По состоянию на август 2021 года фавипиравир не имеет доказательств эффективности по критериям сокращения летальности и риска ИВЛ[6]. По данным низкой достоверности, фавипиравир может снижать время до клинического выздоровления (разрешения симптомов), а также срок госпитализации при COVID-19[62].
На ноябрь 2021 года, по данным исследования PRESECO, фавипиравир не ускоряет выздоровление пациентов с COVID-19. Проводившая исследование канадская биотехнологическая компания признала его бесперспективным против COVID-19[9].
Шесть систематических обзоров, подкрепленных метаанализами, выявили очень слабую доказательную базу в отношении терапевтической эффективности фавипиравира, указывая на то, что в целом он не несет особой пользы для пациентов при лечении COVID-19[63].
Эбола
Клинические испытания по изучению использования фавипиравира против болезни, вызванной вирусом Эбола, начались в гвинейском Гекеду, в декабре 2014 года[64]. Предварительные результаты, представленные в 2016 году на Конференции по ретровирусам и оппортунистическим инфекциям (CROI), опубликованные позднее, показали снижение смертности у пациентов уровень вируса в крови от низкого до среднего, но не влияет на пациентов с высоким уровнем (группа с более высоким риском смерти)[65][66]. Это исследование недостоверно из-за его дизайна — использовался только исторический контроль[67].
Критика
Доктор медицинских наук Василий Власов, профессор НИУ ВШЭ, выступил против применения этого препарата для терапии COVID-19, выразил свои сомнения в эффективности этого препарата и дженериков на его основе[19][68].
Израильский врач доказательной медицины Борис Бриль высказался о фавипиравире как о бесполезном и опасном препарате, за назначение его пациентам в Израиле можно оказаться в тюрьме. Массовое назначение этого препарата в России он объяснил его продвижением финансово заинтересованными людьми[17].
Примечания
- Daniel H. Goldhill, Ada Yan, Rebecca Frise, Jie Zhou, Jennifer Shelley. Favipiravir-resistant influenza A virus shows potential for transmission (англ.) // PLoS pathogens. — 2021-06. — June (vol. 17, iss. 6). — P. e1008937. — ISSN 1553-7374. — doi:10.1371/journal.ppat.1008937. — PMID 34061908.
- Shiraki, K. Favipiravir, an anti-influenza drug against life-threatening RNA virus infections : [англ.] / K. Shiraki, T. Daikoku // Pharmacology & Therapeutics : j. — 2020. — Vol. 209 (May). — Art. 107512. — ISSN 0163-7258. — doi:10.1016/j.pharmthera.2020.107512. — PMID 32097670. — PMC 7102570.
- Furuta, Y. In Vitro and In Vivo Activities of Anti-Influenza Virus Compound T-705 : [англ.] / Y. Furuta, K. Takahashi, Y. Fukuda … [et al.] // Antimicrobial Agents and Chemotherapy. — 2002. — Vol. 46, no. 4. — P. 977—981. — doi:10.1128/AAC.46.4.977-981.2002. — PMID 11897578. — PMC 127093.

- Ibrahim, N. K. Effect of Favipiravir on some epidemic infections: A mini review : [англ.] / N. K. Ibrahim, Z. S. Al-Garawi // Journal of Physics: Conference Series. — 2021. — Vol. 1853. — doi:10.1088/1742-6596/1853/1/012067.
- Łagocka, R. Favipiravir in Therapy of Viral Infections : [англ.] / R. Łagocka, V. Dziedziejko, P. Kłos … [et al.] // Journal of Clinical Medicine. — 2021. — Vol. 10, no. 2. — P. 273. — doi:10.3390/jcm10020273. — PMID 33451007. — PMC 7828521.
- Özlüşen, B. Effectiveness of favipiravir in COVID-19 : a live systematic review : [англ.] / B. Özlüşen, Ş. Kozan, R. E. Akcan … [et al.] // European Journal of Clinical Microbiology & Infectious Diseases. — 2021. — 4 August. — P. 1–9. — ISSN 1435-4373. — doi:10.1007/s10096-021-04307-1. — PMID 34347191. — PMC 8335450.
- Hassanipour, S. The efficacy and safety of Favipiravir in treatment of COVID-19 : a systematic review and meta-analysis of clinical trials : [англ.] / S. Hassanipour, M. Arab-Zozani, B. Amani … [et al.] // Scientific Reports. — 2021. — Vol. 11 (May). — P. 11022. — ISSN 2045-2322. — doi:10.1038/s41598-021-90551-6. — PMID 34040117. — PMC 8155021.
- Фавипиравир внесен в России в список жизненно необходимых препаратов : [арх. 15 октября 2020] // Интерфакс. — 2020. — 14 октября.
- Appili Therapeutics Provides Update on Phase 3 PRESECO Clinical Trial Evaluating Avigan®/Reeqonus™ : [англ.] : [арх. 12 ноября 2021] // Appili Therapeutics. — 2021. — 12 November.
- Jin Z. et al. The ambiguous base-pairing and high substrate efficiency of T-705 (Favipiravir) Ribofuranosyl 5'-triphosphate towards influenza A virus polymerase (англ.) // PLOS One : journal. — Public Library of Science, 2013. — Vol. 8, no. 7. — P. e68347. — doi:10.1371/journal.pone.0068347. — . — PMID 23874596.
- Baranovich T. et al. T-705 (favipiravir) induces lethal mutagenesis in influenza A H1N1 viruses in vitro (англ.) // Journal of Virology : journal. — 2013. — April (vol. 87, no. 7). — P. 3741—3751. — doi:10.1128/JVI.02346-12. — PMID 23325689.
- Guedj J. et al. Antiviral efficacy of favipiravir against Ebola virus: A translational study in cynomolgus macaques (англ.) // PLOS Medicine : journal. — 2018. — March (vol. 15, no. 3). — P. e1002535. — doi:10.1371/journal.pmed.1002535. — PMID 29584730.
- Smee D. F. et al. Intracellular metabolism of favipiravir (T-705) in uninfected and influenza A (H5N1) virus-infected cells (англ.) // The Journal of Antimicrobial Chemotherapy : journal. — 2009. — October (vol. 64, no. 4). — P. 741—746. — doi:10.1093/jac/dkp274. — PMID 19643775.
- Naesens L. et al. Role of human hypoxanthine guanine phosphoribosyltransferase in activation of the antiviral agent T-705 (favipiravir) (англ.) // Molecular Pharmacology : journal. — 2013. — October (vol. 84, no. 4). — P. 615—629. — doi:10.1124/mol.113.087247. — PMID 23907213.
- Shiraki K, Daikoku T (February 2020). “Favipiravir, an anti-influenza drug against life-threatening RNA virus infections”. Pharmacology & Therapeutics. 209: 107512. DOI:10.1016/j.pharmthera.2020.107512. PMID 32097670.
- Pilkington, V. A review of the safety of favipiravir – a potential treatment in the COVID-19 pandemic? : [англ.] / V. Pilkington, V. Pilkington, T. Pepperrell … [et al.] // Journal of Virus Eradication. — 2020. — Vol. 6, no. 2 (April). — P. 45–51. — ISSN 2055-6640. — doi:10.1016/S2055-6640(20)30016-9. — PMID 32405421. — PMC 7213073.
- Катцина, К. «Препараты мракобесия»: израильский врач Борис Бриль — о бесполезных лекарствах для лечения коронавируса : [арх. 17 августа 2021] // NGS24. — 2021. — 17 августа.
- Kimiyasu Shiraki, Tohru Daikoku. Favipiravir, an anti-influenza drug against life-threatening RNA virus infections (англ.) // Pharmacology & therapeutics : journal. — 2020. — 22 February (vol. 209). — P. 107512. — doi:10.1016/j.pharmthera.2020.107512. — PMID 32097670.
- Андрей Заякин. Фавипиравир. Неэффективен и очень опасен. Новая Газета (13 июля 2020).
- FMDA, 2011, p. 3,45: «…favipiravir has the risk of teratogenicity, etc.».
- 条件付き承認で普及に足かせ 富山化学インフル薬の"無念" (яп.). diamond.jp. Дата обращения: 25 февраля 2014.
- Koons, Cynthia. Ebola Drug From Japan May Emerge Among Key Candidates : [англ.] // Bloomberg. — 2014. — 7 August.
- Hayden F. G., Shindo N. Influenza virus polymerase inhibitors in clinical development (англ.) // Current Opinion in Infectious Diseases. — Lippincott Williams & Wilkins, 2019. — Vol. 32, no. 2. — P. 176—186. — doi:10.1097/QCO.0000000000000532. — PMID 30724789.

- Zhang Yangfei. Potential coronavirus drug approved for marketing (англ.). China Daily. Дата обращения: 21 марта 2020.
- Константин Журавлёв. Минздрав одобрил препарат РФПИ и «ХимРара» от коронавируса. Газета.ру (30 мая 2020).
- Государственный реестр лекарственных средств
- Гончаренко Р. Авифавир - новое российское лекарство от коронавируса? / Роман Гончаренко // DW. — 2020. — 11 июня.
- Du,, Y.‐X. Favipiravir : pharmacokinetics and concerns about clinical trials for 2019-nCoV infection : [англ.] / Y.‐X. Du,, X.‐P. Chen // Clinical pharmacology and therapeutics : j. — 2020. — April. — doi:10.1002/cpt.1844. — PMID 32246834.
- Swift R. Fujifilm's Avigan inconclusive in COVID-19 patients in Japan trial : [англ.] : [арх. 10 июля 2020] / Reporting by Rocky Swift; Editing by Chris Gallagher and Chang-Ran Kim // Reuters. — 2020. — 10 July.
- Теслина А. Фавипиравир не показал убедительной эффективности при COVID-19 / Анастасия Теслина // Фармвестник. — 2020. — 10 июля.
- MediVector Completes Patient Enrollment In Two Phase 3 Studies Of Favipiravir For Influenza. BioSpace. Дата обращения: 5 мая 2020.
- Lumby, Casper (3 March 2020). “Favipiravir and Zanamivir Cleared Infection with Influenza B in a Severely Immunocompromised Child”. Clinical Infectious Diseases. 71 (7): e191—e194. DOI:10.1093/cid/ciaa023. PMID 32124919.
- Hayden FG, Shindo N (April 2019). “Influenza virus polymerase inhibitors in clinical development”. Current Opinion in Infectious Diseases. 32 (2): 176—186. DOI:10.1097/QCO.0000000000000532. PMC 6416007. PMID 30724789.

- Conditional approval hampers popularization Toyama Chemical's flu drug "remorse" (яп.). Дата обращения: 25 февраля 2014.
- Coronavirus, il Veneto sperimenta l'antivirale giapponese Favipiravir. Ma l'Aifa: "Ci sono scarse evidenze scientifiche su efficacia" (итал.). Il Fatto Quotidiano (22 марта 2020). Дата обращения: 23 марта 2020.
- Yangfei, Z. Potential coronavirus drug approved for marketing : [англ.] // China Daily. — 2020. — 17 March.
- Glenmark Launches COVID-19 Drug Favipiravir At ₹ 103 Per Tablet : [англ.] // NDTV. — 2020. — 21 June.
- Первый препарат против COVID-19 «Авифавир» поступил в клиники семи регионов РФ. Интерфакс (11 июня 2020). Дата обращения: 15 ноября 2020.
- Russian Ministry of Health approves the first COVID-19 drug Avifavir produced by JV of RDIF and ChemRar, RDIF (30 May 2020). Дата обращения 31 мая 2020.
- Russian Health Ministry approves anti-coronavirus drug Avifavir, BNN Bloomberg (31 May 2020). Дата обращения 31 мая 2020.
- Russia plans coronavirus vaccine clinical trials in two weeks - report, Reuters (30 May 2020). Дата обращения 31 мая 2020.
- Минздрав одобрил препарат от коронавируса «Арепливир» : [арх. 26 июня 2020] // Интерфакс. — 2020. — 25 июня.
- Минздрав РФ одобрил третий препарат для лечения коронавируса. Интерфакс (8 июля 2020). Дата обращения: 15 ноября 2020.
- 'FabiFlu is the most economical COVID-19 treatment option': Glenmark's reply to Centre on alleged 'overpricing'. DNA India (21 July 2020). Дата обращения: 22 июля 2020.
- Favipira - Tablet - 200 mg - Beacon Pharmaceuticals Ltd. - Indications, Pharmacology, Dosage, Side Effects & other Generic Info. Medex. Дата обращения: 22 июля 2020.
- T-705 (favipiravir) and related compounds: Novel broad-spectrum inhibitors of RNA viral infections (англ.) // Antiviral Research : journal. — 2009. — June (vol. 82, no. 3). — P. 95—102. — doi:10.1016/j.antiviral.2009.02.198. — PMID 19428599.
- Фавипиравир (Favipiravirum)- описание вещества, инструкция, применение, противопоказания и формула.. www.rlsnet.ru. Дата обращения: 1 декабря 2021.
- Center for Food Safety and Applied Nutrition. Redbook 2000: IV.C.1. Short-Term Tests for Genetic Toxicity (англ.). U.S. Food and Drug Administration (11 апреля 2019). Дата обращения: 14 января 2022.
- FMDA, 2011, p. 44.
- Khambholja & Asudani, 2020.
- FMDA, 2011, p. 1,172.
- Gatherer D. The 2014 Ebola virus disease outbreak in West Africa (англ.) // Journal of General Virology. — Microbiology Society, 2014. — August (vol. 95, no. Pt 8). — P. 1619—1624. — doi:10.1099/vir.0.067199-0. — PMID 24795448.

- Smither S. J. et al. Post-exposure efficacy of oral T-705 (Favipiravir) against inhalational Ebola virus infection in a mouse model (англ.) // Antiviral Research. — 2014. — April (vol. 104). — P. 153—155. — doi:10.1016/j.antiviral.2014.01.012. — PMID 24462697.
- Cohen J. Results from encouraging Ebola trial scrutinized : [англ.] // Science Insider : электр. ресурс. — 2015. — February. — doi:10.1126/science.aaa7912.
- Khambholja & Asudani, 2020, Table 1.
- Zhejiang Hisun Pharma gets approval for clinical trial to test flu drug Favipiravir for pneumonia caused by new coronavirus. Reuters Healthcare, February 16, 2020.
- Fujifilm Announces the Start of a Phase III Clinical Trial of Influenza Antiviral Drug Avigan (favipiravir) on COVID-19 in Japan and Commits to Increasing Production (англ.). Drugs.com. Дата обращения: 12 апреля 2020.
- Coronavirus, il Veneto sperimenta l'antivirale giapponese Favipiravir. Ma l'Aifa: "Ci sono scarse evidenze scientifiche su efficacia" (итал.). Il Fatto Quotidiano (22 марта 2020). Дата обращения: 23 марта 2020.
- Яланская А. Что известно о зарегистрированном для лечения COVID-19 препарате «Авифавир» / Анастасия Яланская // Парламентская газета. — 2020. — 1 июня.
- «Р-Фарм» и «Промомед» начали КИ фавипиравира от COVID-19. Vademecum (22 мая 2020). Дата обращения: 29 июня 2020.
- COVID-19 : Informal consultation on the potential inclusion of Favipiravir in a clinical trial : Draft : [англ.]. — Geneva : WHO, 2020. — 10 April. — 19 p. — (WHO R&D Blueprint).
- Siemieniuk, R. A. C. Drug treatments for covid-19: living systematic review and network meta-analysis : [англ.] / R. A. C. Siemieniuk, J. J. Bartoszko, L. Ge … [et al.] // BMJ. — 2020. — Vol. 370 (30 July). — M2980. — ISSN 1756-1833. — doi:10.1136/bmj.m2980. — PMID 32732190. — PMC 7390912.
- Р. Дмитриев. Лечение коронавируса. Помогает ли фавипиравир при ковиде так, как хотелось бы?. Какую пользу следует ожидать от фавипиравира в борьбе с коронавирусом. Mosmedpreparaty.ru. «Мосмедпрепараты» (15 ноября 2021).
- Guinea: Clinical Trial for Potential Ebola Treatment Started in MSF Clinic in Guinea. AllAfrica – All the Time. Дата обращения: 28 декабря 2014.
- Sissoko D, Laouenan C, Folkesson E, M'Lebing AB, Beavogui AH, Baize S, et al. (March 2016). “Experimental Treatment with Favipiravir for Ebola Virus Disease (the JIKI Trial): A Historically Controlled, Single-Arm Proof-of-Concept Trial in Guinea”. PLOS Medicine. 13 (3): e1001967. DOI:10.1371/journal.pmed.1001967. PMC 4773183. PMID 26930627.
- Fink, Sheri. Ebola Drug Aids Some in a Study in West Africa, The New York Times (4 February 2015).
- Cohen, Jon (26 February 2015). “Results from encouraging Ebola trial scrutinized”. Science. DOI:10.1126/science.aaa7912. Дата обращения 21 January 2016.
- «Это бизнес, это не имеет отношения к науке и фармацевтике»: доктор медицины о препарате от COVID-19 : [видео]. // Навальный Лайф. — 2020. — 25 сентября.
Литература
- Khambholja, K. Potential repurposing of Favipiravir in COVID-19 outbreak based on current evidence : [англ.] / Kapil Khambholja, Deepak Asudani // Travel Medicine and Infectious Disease. — 2020. — Vol. 35. — P. 101710. — 2 p. — ISSN 1477-8939. — doi:10.1016/j.tmaid.2020.101710. — PMID 32360327. — PMC 7252084.
- Report on the deliberation results – avigan : [англ.] / Evaluation and Licensing Division, Pharmaceutical and Food Safety Bureau. — Japan : Pharmaceuticals and Medical Devices Agency, 2011. — 172 p.
Документы
- Регистрационное удостоверение ЛП-006225 : Авифавир // Государственный реестр лекарственных средств. — Минздрав РФ, 2020. — 29 мая.
- Регистрационное удостоверение ЛП-006288 : Арепливир // Государственный реестр лекарственных средств. — Минздрав РФ, 2020. — 23 июня.
- Блинов, А. А. Инструкция по медицинскому применению лекарственного препарата Авифавир : ЛП-006225-290520 / ООО «Кромис». — Министерство здравоохранения Российской Федерации, 2020. — 29 мая. — 8 с.
Ссылки
- Drug Name: Favipiravir [USAN:INN:JAN] (англ.). Drug Information Portal. U. S. National Library of Medicine.